By Lisandra Paraguassu – Reuters
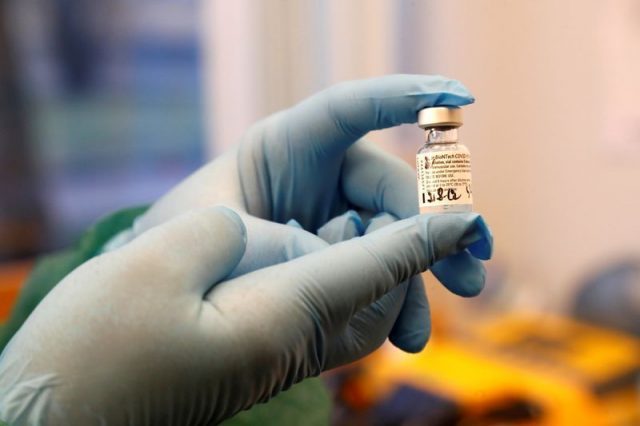
A Agência Nacional de Vigilância Sanitária (Anvisa) concedeu na segunda-feira o certificado de boas práticas de fabricação ao laboratório Pfizer, etapa necessária para o registro da vacina contra Covid-19 desenvolvida pelo laboratório no país.
De acordo com a Anvisa, a Pfizer utiliza quatro empresas na produção do ativo biológico usado na sua vacina, e a agência já tem informações suficientes sobre três delas, faltando apenas a complementação da quarta.
A Pfizer, que desenvolveu uma vacina em parceria com a alemã BioNTech, é a terceira empresa fabricante de vacinas contra a Covid-19 a receber o certificado de boas práticas visando o registro do imunizante no país. A primeira delas foi a chinesa Sinovac e a segunda, a AstraZeneca.
Nenhuma das empresas, no entanto, pediu até agora o registro emergencial de suas vacinas. Todas as três estão usando por enquanto a submissão contínua –processo em que os laboratórios apresentam os dados e documentos necessários para o registro a medida que eles vão sendo obtidos, para que sejam analisados antecipadamente, acelerando assim a concessão do registro no final.
A Pfizer informou que não pretende pedir o registro emergencial criado pela Anvisa com base em medidas adotadas em outros países. A empresa negocia um contrato de venda de 70 milhões de doses da sua vacina para o governo brasileiro, que ainda não está fechado.
O pedido de registro emergencial exige das empresas a apresentação de quantas doses e qual o cronograma de aplicação no país. A empresa alega que isso só poderá ser feito com o contrato em definitivo, que o governo até agora não assinou.
Na segunda-feira, o presidente Jair Bolsonaro cobrou que as empresas que querem vender vacinas contra a Covid-19 ao Brasil apresentem a documentação para a Anvisa.
“O Brasil tem 210 milhões de habitantes, então um mercado de consumidor de qualquer coisa enorme. Os laboratórios não tinham que estar interessados em vender para a gente? Por que eles não apresentam documentação na Anvisa?”, disse.
Um dos problemas para a assinatura do contrato de venda da Pfizer, no entanto, é a resistência do presidente a um artigo em que o laboratório diz que não se responsabiliza por eventuais efeitos colaterais –o artigo é padrão em bulas e contratos de venda de medicamentos, mas Bolsonaro não quer que o governo brasileiro assuma o risco.